Una de cada seis parejas en España tiene problemas para tener hijos. Muchas recurren a técnicas de reproducción asistida como la fecundación in vitro, un tratamiento complejo para unir el óvulo con un espermatozoide en el laboratorio. El objetivo es obtener embriones de buena calidad que, tras transferirlos al útero materno, puedan fructificar en un embarazo. La técnica funciona, pero existe todo un rosario de complementos que no tiene por qué hacerlo. Como respuesta a la creciente demanda, la medicina reproductiva ha investigado docenas de complementos para mejorar el resultado, y algunas clínicas los ofrecen aunque no siempre estén respaldados por suficiente evidencia científica. Es el caso de procedimientos tan dispares como “la eclosión asistida” o “el pegamento embrionario”, que prometen aumentar las posibilidades de tener un bebé sin contar con estudios suficientes que los avalen, según advierte una serie de artículos científicos de la Sociedad Estadounidense de Medicina Reproductiva que ha visto la luz en la revista Fertility and Sterility.
“El único objetivo que tiene gran parte de estos métodos es sacar dinero. Se aprovechan de la tormenta perfecta de que miles de parejas están desesperadas y tienen una ansiedad increíble por encontrar tratamientos milagrosos. Se juega con la desesperación de la paciente con campañas de marketing, se falsean las cifras de los tratamientos y colocan a la gente cualquiera de estos métodos. Al final tenemos una población cautiva de la mala praxis médica, en la que entra un factor externo como el negocio”, sentencia el ginecólogo Rafael Bernabeu, director médico del Instituto Bernabeu y director de la cátedra de Medicina Reproductiva de la Facultad de Medicina de la Universidad Miguel Hernández de Elche.
La fecundación in vitro, recuerda este experto, trabaja con embriones humanos que anidan en un porcentaje menor de lo deseado, en el que el proceso de implantación es todavía desconocido. “Solo tenemos información fraccionaria de algún aspecto que puede mejorar con algún tratamiento, pero lo demás está basado en un interés de la medicina compasiva: la paciente pide algo y se le da un placebo para que se vaya más tranquila a casa”, señala Bernabeu. Estos son los complementos que las nuevas investigaciones han señalado como carentes suficiente base científica que asegure su eficacia.
La eclosión asistida no garantiza más probabilidades
El embrión está rodeado de una corteza, la zona pelúcida, que debe romper para anidar en el útero. En la actualidad, la eclosión asistida requiere el uso de un láser -antes solía aplicarse ácido- para disgregar parte de esa cápsula, que se pule como si se tallara un diamante para hacer un orificio en la membrana. El objetivo es que el embrión salga y se implante en el útero. La eclosión (también conocida como hatching) asistida resulta efectiva cuando forma parte de un procedimiento para extraer una muestra del tejido embrionario.
“El embrión extruye a través del orificio algunas células de la futura placenta. A los tres días, estas células se recogen y se hace una biopsia para estudiar la composición cromosómica del embrión para evitar implantaciones que solo provoquen un aborto o anomalías”, describe Bernabeu. El problema es que la técnica del hatching asistido no cuenta con la suficiente evidencia científica para apoyar su uso generalizado, no mejora los resultados del embarazo. “Solo es una etapa previa para realizar una biopsia al embrión, pero no garantiza más posibilidades de embarazo”, advierte el ginecólogo.
El examen genético preimplantacional no es para todas
El ovario clasifica los ovocitos por competencia biológica. Los primeros en liberarse corresponden a los más competentes, lo que explica la alta tasa de embarazos en la adolescencia y el ínfimo porcentaje de abortos y nacimientos de niños afectados por anomalías. Con la edad, la curva de la fertilidad desciende, con una caída dramática a partir de los 35 años. Pasados los 40, cuatro de cada cinco embriones serán anómalos o aneuploides, es decir, con un número de cromosomas incorrecto. El examen genético preimplantacional, también conocido por sus siglas en inglés PGT-A, permite saber si los cromosomas que dirigen las divisiones celulares tienen el número adecuado. “Ahora hay forma de discernir si puede dar a un síndrome de Down o si es sano, aunque el aspecto de ambos embriones sea idéntico”, destaca Bernabeu.
A los dos días, el embrión empieza a extruir células, y se toman muestras para analizarlas a través de la eclosión asistida. “Inicialmente, las primeras biopsias se hacían a los tres días de vida, cuando el embrión consta solo de ocho células. La técnica implica arrancar una o dos células, por lo que es muy agresiva en una etapa temprana tan vulnerable. Es mejor aplicar un PGT-A a los cinco o seis días, al haber más células”, aconseja este ginecólogo. En caso de mujeres de 30 años, la posibilidad de que el número de cromosomas sea anormal es muy reducida, por lo que se desaconseja realizar este examen. “El PGT-A se indica en casos de edad de maternidad avanzada, de abortos de repetición, de factor masculino severo y de causas desconocidas, en los que todo parece estar bien, pero la mujer no gesta. Universalizarlo no tiene sentido. Los casos de mujeres con un nivel cromosómico normal, aunque tengan 40 años, tendrán las mismas posibilidades que cuando tenían 20″, señala el experto.
Sistema ‘Time-lapse’, ¿para qué tantas fotos?
Basada en un sistema de incubación, este método consiste en tomar fotos del embrión de forma periódica para realizar una secuencia de imágenes en la que se observa la división celular del embrión. A pesar de que existan diversos sistemas comercializados, no cuenta con la evidencia que fundamente su utilización, y solo supone un incremento de coste en el tratamiento. “Esta tecnología solo puede evaluar embriones por debajo de tres días de desarrollo, y hay que tener en cuenta que los transferimos al quinto o sexto día. No hay todavía un volumen de evidencia para sostener su efectividad”, explica Bernabeu.
Pegamento embrionario, un adhesivo que no pega
Aunque su nombre resulte muy atractivo para las pacientes que desean lograr el embarazo, hay que desengañarse. No existe un pegamento para adherir el embrión, por mucho que quienes publiciten esta técnica la describan como una sustancia con altos niveles de ácido hialurónico que ayuda a que el útero se torne más pegajoso, lo que ayuda a que se implante el embrión. “El embryo glue, o pegamento embrionario, no sirve para nada. Su nombre induce a error porque parece que se pueda adherir el embrión con pegamento. Estamos preparando un artículo que se encuentra en fase de publicación, el cual se suma a otros trabajos publicados, y coincidimos que no aumenta la tasa de embarazo”, sentencia Bernabeu.
Rascado endometrial, un procedimiento en entredicho
Durante mucho tiempo, clínicas como la del ginecólogo Bernabeu han aplicado esta técnica basada en un estudio publicado en 2003 por un grupo de investigación israelí. El endometrio, la mucosa que recubre el interior del útero, lo compone por un tejido esponjoso repleto de sangre, glucógeno, hidratos y demás elementos que el embrión necesita. La hipótesis inicial partía de que, si se labra un surco, se crea una herida en el endometrio que luego vuelve a cubrirse, y ese proceso de reparación podría aumentar la receptividad y explicar un incremento en la tasa de embarazo. Desafortunadamente, los estudios publicados desde entonces son contradictorios. “Hay trabajos que demuestran que puede haber una mejoría y otros en los últimos años, por el contrario, señalan que el rascado o scratching no mejora los resultados”, reconoce Bernabeu. El rascado se aconseja en algunos casos de mujeres con fallos de implantación reiterados sin causa conocida.
No daña, pero ¿ayuda la vasodilatación?
Los vasodilatadores de la arteria uterina para aumentar el aporte de sangre en dicha arteria a través de vasodilatadores que, al relajar los vasos sanguíneos, disminuyen la resistencia. “En algunos casos de mujeres que ya han pasado por varios fracasos con tratamientos y tienen el reducido riego sanguíneo, indicar vasodilatadores puede tener su lógica y puede mejorar, aunque no está claramente comprobado”, apunta Bernabeu. Los especialistas han llegado a utilizar la Viagra para conseguirlo, pero no han tenido éxito, recuerda el ginecólogo. “Se han empleado otros fármacos vasodilatadores con la posibilidad de aumentar algo el flujo de sangre al útero y mejoran la irrigación de la cavidad, pero no deja de ser todavía una hipótesis de trabajo”. Lo único bueno es que son tratamientos que no tienen efectos secundarios, no son costosos económicamente y son bien tolerados.
Activación artificial de óvulos, un concepto aventurado
Las mujeres solo pueden producir ovocitos durante tres meses en toda su vida, desde la semana undécima del embarazo a la semana vigesimosegunda o vigesimotercera, es decir, del tercer al quinto mes de gestación. A partir de los 40 años se pierden los ovocitos que puedan dar lugar a embarazo, y entra una confrontación entre lo que la biología dictamina y la sociedad permite. “Si se pospone la maternidad, las pacientes nos piden ayuda cuando tienen agotada su dotación de ovocitos, pueden quedar óvulos pero no son fertilizables, o pueden dar lugar a anomalías o abortos con un porcentaje muy alto”, explica el especialista.
A pesar de que la desesperación tanto de pacientes como de médicos por generar ovocitos -creados a partir de otras partes del organismo o en cultivo- ha llevado a investigar esta línea de trabajo de forma insistente en los últimos doce años, todavía no se ha aplicado en humanos. “Sin embargo, todavía no hemos sido capaces de generar ovocitos, son trabajos experimentales. El problema es que todas las células tienen 46 cromosomas, excepto dos, en el testículo y en el ovario, donde se reducen a la mitad. Esa reducción todavía es fruto de la especulación científica. Decirle hoy a una mujer que se le puede implantar ovocitos artificiales no tiene ningún soporte médico ni científico”, recalca este especialista en medicina reproductiva.
La inmunoterapia, solo en caso de enfermedad
Una de las variantes de esta técnica corresponde a la inmunoterapia con linfocitos, desarrollada para mujeres con pérdida recurrente del embarazo sin causa aparente. Está prohibida por la Administración de Alimentos y Medicamentos de Estados Unidos (FDA, por sus siglas en inglés) y, sin la recomendación de la Organización Mundial de la Salud, solo se practica en contados centros privados de Latinoamérica, Asia y Europa. El tratamiento consiste en aplicarle a la paciente inyecciones intradérmicas compuestas de glóbulos blancos del futuro padre, lo que provoca una supuesta reacción en su sistema inmunológico que ayuda a la aceptación del bebé. El coste de las dosis, que también pueden administrarse cada tres o cuatro semanas durante la gestación para mantener activa la reacción inmunológica, puede alcanzar los 1.300 euros.
Las técnicas de inmunoterapia están exclusivamente indicadas en casos de enfermedades inmunitarias que afectan a la madre. “Todo lo demás es fruto de la falacia”, advierte Bernabeu. En caso de que no existan problemas con el sistema inmune, la aplicación de esta terapia no cuenta con evidencia que avale su beneficio. “Se han administrado corticoides, inmunosupresores o tratamientos sobre la base de una hipotética posibilidad de lo que se llama el rechazo embrionario. Si se le dice a una paciente que es posible que su cuerpo rechace el embrión y que le dará un tratamiento para que no ocurra, la mujer lo querrá, pero no está demostrado que funcione”, explica el ginecólogo.
Infusiones intralipídicas, solo placebo
Relacionada con la inmunoterapia, esta técnica surgió de la inspiración de algunos investigadores al observar que, en algunos casos, la alimentación intravenosa en pacientes con dificultades para nutrirse por vía oral mejoraba su sistema inmune. “Se pensó que se podría aplicar a pacientes sanos, por ejemplo, a mujeres en tratamientos de fecundación in vitro antes de transferir el embrión”, explica Bernabeu. Se trata de modular la respuesta inmunitaria materna en la llegada de un embrión, que es entendido como un elemento externo al sistema inmunitario. “Esta vía debería permitir que, durante el tiempo de transferencia, el sistema inmune no estuviera tan activo, pero solo es una suposición teórica”, recalca Bernabeu.
Las infusiones intralipídicas se han utilizado en pacientes con las que otros métodos han fracasado estrepitosamente. “Las infusiones se indican para casos muy concretos de enfermedades inmunes, usarlas sistemáticamente es aprovecharse de los pacientes sin justificación”, apunta Bernabeu. Se trata de un tratamiento compasivo, o placebo, al igual el uso de la heparina, que es un anticoagulante como la aspirina -también se ha planteado en ciertos casos-, pero hay trabajos que dicen que mejora, y otros estudios lo niegan. “Depende del grupo de población. No es lo mismo una pareja que lleva cinco años con tratamiento a la que lleva un año, puede que en el primero pueda experimentar una mejora”, señala Bernabeu.
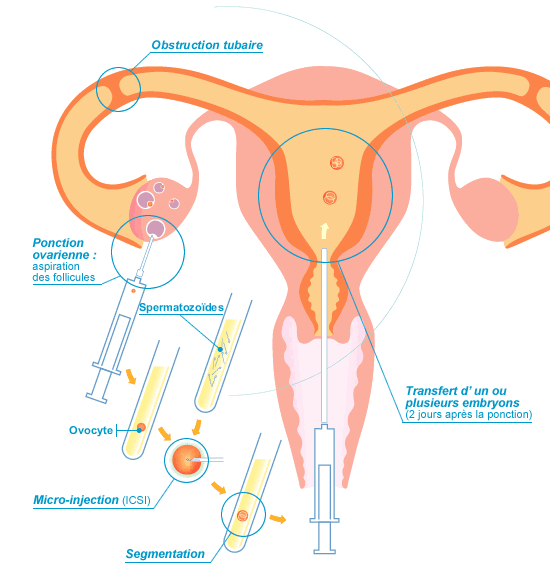
Una infructuosa inyección intracitoplásmica
El funcionamiento de este método consiste en microinyectar un único espermatozoide directamente en el interior del ovocito para conseguir su fecundación. Se aconseja en casos de factor masculino severo, cuando el futuro padre tiene una calidad seminal muy baja o por problemas de causa desconocida. “Por su rapidez y comodidad, hay laboratorios que la hacen a todas las parejas, pero es un método agresivo que tiene sus indicaciones y limitaciones”, observa Bernabeu. Similar a esta técnica, la inyección intracitoplasmática de espermatozoides morfológicamente seleccionados, basada en que un microscopio seleccionaba el mejor espermatozoide y conseguía aumentar la fertilidad, resultó infructuoso. “Fue un ‘bluf’, no servía en absoluto. Se replicaba y no funcionaba”, recuerda este experto.
El incompleto test de receptividad endometrial
No es infrecuente que las mujeres que se han sometido a un buen número de tratamientos busquen información acera de esta técnica en Internet. El test de receptividad endometrial, que se ofrece a un precio que oscila entre los 300 y 900 euros, promete hacer un análisis para saber cuál es el mejor momento para implantar el óvulo. Pero cuenta con dos importantes limitaciones para que se aplique en la práctica médica. Por un lado, no se ha encontrado un panel de genes que discrimine con suficiente claridad un endometrio receptivo; por el otro, hay que evaluar su papel en pacientes que sufren fallos repetidos de implantación embrionaria, dado que hasta un cuarto de estas pacientes puede tener una ventana de implantación adelantada o retrasada. “En estos momentos, adolece de trabajos bien diseñados que demuestren sus beneficios”, advierte Bernabeu.
.